
近日,青岛大学两位“泰山学者”教授团队相继聚焦癌症放疗增敏与精准催化治疗领域,突破现有技术瓶颈,为癌症精准治疗提供全新思路。
青岛大学附属烟台毓璜顶医院耳鼻咽喉头颈外科宋西成教授团队,在Molecular Cancer(中科院1区TOP期刊,最新IF=33.9)发表题为“Platinum-Based Functional Nanomaterials: Mechanisms and Therapeutic Strategies in Cancer Radiotherapy Sensitization”(《铂基功能纳米材料:在癌症放疗增敏中的机制和策略》)的综述论文。该论文聚焦铂基功能纳米材料在癌症放射治疗增敏方面的前沿进展,系统整合了该领域的零散研究,填补了纳米放射生物学视角下的全面认知空白。
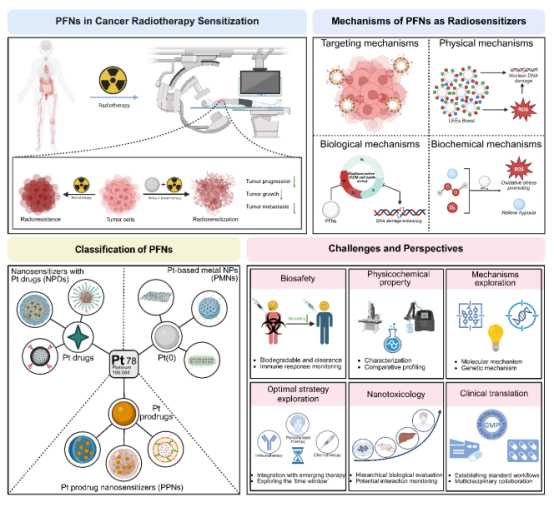
铂基功能纳米材料在放疗增敏中的机制、分类、挑战和应用前景概要(图源:Yuanchao Cheng et al. Mol Cancer. 2025)
宋西成教授团队在论文中全面总结了铂基功能纳米颗粒从物理剂量增强效应到生物调控效应的多维度作用机制,将铂基功能纳米材料明确分为铂基金属纳米颗粒、铂类药物纳米增敏剂和铂前药纳米增敏剂三大类,分别剖析了各类材料在肿瘤放射治疗中的研究现状、核心优势与现存不足,并清晰指明了该领域的未来发展方向。
论文明确提出,通过材料科学、放射生物学和临床医学的多学科交叉融合,有望突破现有铂基功能纳米颗粒在合成优化、靶向递送和临床转化等方面的瓶颈,为开发新一代高效低毒的纳米放疗增敏剂提供坚实的理论指导和关键技术支持,最终实现肿瘤精准放射治疗的临床突破。该研究是宋西成教授团队推进国家临床重点专科、山东省耳鼻喉疾病临床医学研究中心和山东省神经免疫互作与调控重点实验室建设的重要实践,相关研究得到国家自然科学基金、山东省重点研发计划(竞争创新平台项目)、“泰山学者计划”项目、中国博士后科学基金面上资助和山东省自然科学基金等多项国家级、省级项目的资助支持。
青岛大学慢病研究院付钦瑞教授课题组,在ACS Nano(中科院1区,IF=16.1)发表题为“Self-Propelled Nanoreactors for Enhanced Cascade Catalytic Cancer Therapy through NIR-II Fluorescence Imaging-Guided Readministration”的研究成果,创新性设计了一种自驱动纳米反应器(DSFGC),有效破解了传统催化治疗的多项核心技术瓶颈,为癌症精准催化治疗提供了新方案。
催化治疗凭借其精准靶向、高效安全及成本可控等优势,已成为癌症治疗领域的研究热点,展现出巨大临床潜力,但传统纳米反应器存在四大核心瓶颈,严重制约其治疗效果:一是肿瘤组织穿透能力有限,难以到达深部肿瘤细胞;二是肿瘤微环境中过氧化氢浓度不足,无法满足催化反应需求;三是单次给药治疗效果有限,难以彻底清除肿瘤细胞;四是再次给药时机难以精准判断,易导致给药过量或不足,影响治疗效果且可能增加毒副作用。
为针对性解决上述问题,付钦瑞教授团队设计的自驱动纳米反应器(DSFGC)通过Pickering乳液法成功构建,具有Janus不对称结构,整合了第二近红外(NIR-II)荧光纳米颗粒、类过氧化物酶纳米酶(FePt纳米酶)以及不对称修饰的过氧化氢酶(CAT)和葡萄糖氧化酶(GOx),兼具自驱动、级联催化与成像引导给药三大核心功能,实现了“诊断-治疗-监测”一体化。
该纳米反应器的作用机制具有明确的级联协同效应,且经过体外细胞实验、体内动物实验充分验证:在肿瘤微环境中,过表达的过氧化氢首先被过氧化氢酶(CAT)催化分解为氧气,一方面,氧气气泡驱动纳米反应器自主运动,显著提升其向深部肿瘤组织的渗透能力,有效解决了传统纳米反应器穿透不足的难题;另一方面,氧气作为葡萄糖氧化酶(GOx)的反应底物,可显著增强GOx的催化活性,促进其高效消耗肿瘤细胞内的葡萄糖,生成葡萄糖酸并自补充过氧化氢,既实现了“饥饿疗法”(剥夺肿瘤细胞能量供应,抑制肿瘤增殖),又解决了肿瘤微环境中过氧化氢浓度不足、难以支撑催化反应的核心痛点。随后,生成的葡萄糖酸会进一步酸化肿瘤微环境,激活类过氧化物酶纳米酶(FePt纳米酶)的催化活性,促进高毒性羟基自由基(·OH)的生成,实现化学动力学疗法(CDT)对肿瘤细胞的精准杀伤,最终达成饥饿疗法与化学动力学疗法的协同增效,大幅提升肿瘤治疗效果。
更为关键的是,该纳米反应器保留了核心材料在1550 nm处的强NIR-II荧光发射能力,借助NIR-II荧光成像技术,可实时、精准监测纳米反应器在肿瘤内的富集、分布及代谢动态,进而精准获取最佳再给药窗口——实验证实,首次给药后27小时与60小时为最佳再给药时机。通过成像引导精准再给药,既能进一步提升肿瘤治疗效果,又能有效降低药物对正常组织的损伤,显著提高治疗的安全性。体外细胞实验显示,该纳米反应器可引发显著的活性氧(ROS)爆发,导致肿瘤细胞DNA双链断裂,诱导的肿瘤细胞凋亡率高达63.8%,显著优于单一组分或部分组合治疗方案;活体动物实验证实,该系统可显著抑制肿瘤生长、缩小肿瘤体积,有效延长实验小鼠生存期,且具有良好的生物相容性与安全性,为后续临床转化奠定了坚实基础。
该研究由青岛大学2022级细胞生物学研究生王梦真和2022级博士研究生江泽宇担任并列第一作者,付钦瑞教授为论文通讯作者,青岛大学为唯一完成单位,研究得到“泰山学者计划”等项目的资助支持。